국내외 제품 인허가 및 품질 시스템 인증 전문 컨설팅 와이즈컴퍼니(주)입니다.
와이즈컴퍼니(주)는 국내 최초로 인도 GLP 시험소와 협력하여 FDA ASCA, FDA GLP(21 CFR Part 58) 및 OECD GLP 기준을 엄격히 준수하는 글로벌 수준의 생체적합성 시험 서비스를 제공하고 있습니다.
지금까지 수천 건의 시험 보고서를 성공적으로 완료하였으며, 해당 보고서들은 각국 규제기관에서 신뢰도 높은 근거 자료로 활용되고 있습니다.
이번 포스팅에서는 여러 제품 중 콘택트렌즈(Contact Lens) 제품의 생체적합성 시험 수행 후기를 공유드립니다.
인도 시험소 이슈 및 대응
본 건은 2024년 2월 공표된 ‘Fraudulent and Unreliable Laboratory Testing Data’ 레터로 인해 인도 내 시험 보고서에 대한 510(k) 인증 거절 우려가 제기된 사례였습니다.
그러나 해당 이슈는 일부 GLP 미준수 시험소에 국한된 문제였으며, 당사는 관련 규정을 철저히 준수했음을 소명하여 2025년 7월 510(k) 인증을 성공적으로 완료하였습니다.

FDA 공표 자료에 따르면, FDA ASCA 공인 시험소 이용이 신뢰 가능한 대안으로 명시되어 있으며, 파트너 시험소는 FDA ASCA 인증 시험기관으로 국내외 비인증 시험소 대비 높은 규제 신뢰성을 확보하고 있습니다.
접촉 분류 및 시험 항목
ISO 10993-1에서는 누적 접촉 및 반복 사용을 고려하여 최종 인체 접촉 분류를 설정하도록 요구하고 있습니다.

- 누적 접촉: 동일 환자에게 동일 장비가 연속적으로 2회 이상 사용
- 반복 사용: 동일 환자에게 서로 다른 신규 장비가 연속적으로 2회 이상 사용
이를 고려할 때 대상 콘택트렌즈 제품은 다음과 같이 분류됩니다.
접촉 분류: Surface device / Mucosal membrane / Prolonged or Long-term
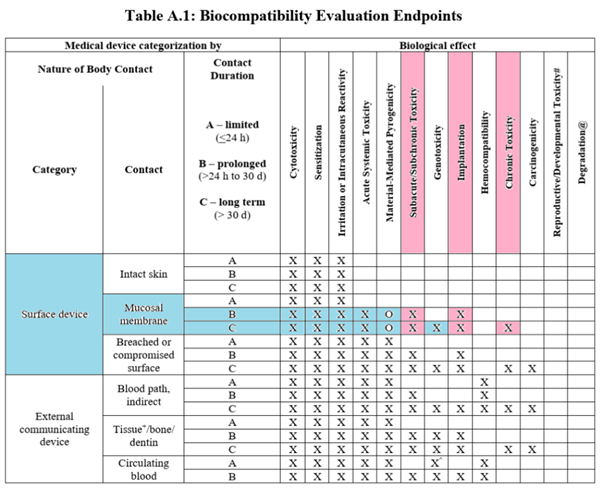
일부 시험 항목은 시험 설계 변수(시험 기간, 동물 종류, 방법)가 많아 사전 규제 전문가 협의가 필수입니다.
주요 생체적합성 시험 항목
| 번호 | 시험 항목 | 적용 규격 |
|---|---|---|
| 1 | 세포독성 (Cytotoxicity) | ISO 10993-5 |
| 2 | 피부감작성 (Sensitization) | ISO 10993-10 / GMPT |
| 3 | 안자극 (Ocular Irritation) | ISO 10993-23 |
| 4 | 급성독성 | ISO 10993-11 |
| 5 | 물질매개발열성 | ISO 10993-11 / USP <151> |
| 6 | 아만성독성 | ISO 10993-6 / 10993-11 |
| 7 | 유전독성 | ISO 10993-3 / 10993-33 |
| 8 | 염색체 이상 시험 | ISO 10993-3 / 10993-33 |
| 9 | 이식 시험 (토끼 안구) | ISO 9394 |
| 10 | 만성독성 | ISO 10993-11 |
ISO 10993 vs FDA 가이던스 차이
인허가 대상 국가에 따라 요구 시험 항목은 달라질 수 있습니다.
- ISO 10993 기준: 전체 생체적합성 매트릭스 적용
- FDA 가이던스 기준: 콘택트렌즈 및 1차 포장재 중심 시험 요구
아만성·만성독성 시험 전략
아만성 및 만성독성 시험은 비용과 기간 부담이 크기 때문에, 다수 제조사는 화학적 특성화 및 독성학적 위험평가 기반의 생물학적 평가로 시험 제외 전략을 수립하고 있습니다.
시험 진행 프로세스
계약 체결
시험 범위 및 규제 요구사항 확정
시료 도착 및 검수
시험소 내 시료 적합성 확인
시험 플랜 수립 및 승인
프로토콜 준비(약 3~4주) 후 승인 절차 진행
시험 수행 및 보고서 발행
초안 검토 후 서명 포함 최종 보고서 발행(2~4주)
와이즈컴퍼니(주)는 시험 수행뿐 아니라 규제기관 코멘트 대응 및 지원사업 서류까지 포함한 전주기 컨설팅을 제공합니다.